Изомерия. Виды изомерии
Геометрическими изомерами являются цис-транс-изомеризм, или изомеризм EZ. Их действия основываются на ограниченном вращении двойных или одинарных углеродных связей в циклических соединениях.В циклическом соединении, вращение между углеродной одинарной связью ограничено и две различные группы присоединены к каждой углеродной изомерии аналогичным образом. Такие геометрические изомеры часто отличаются по своим физическим свойствам. Это связано с формой изомеров и общим дипольным моментом. Если два атома с наивысшим приоритетом остаются на той же стороне изомера, то они обозначаются как Z, и если они находятся в противоположной стороне - E.
Краткая история изомерии
Концепция конституционной изомерии - это значительный шаг вперед в истории современной химии и, особенно в развитии органической химии. Уже к концу 1700-х годов было выделено несколько чистых веществ путем изучения «животной» и «растительной» химии. Многие были получены Карлом Вильгельмом Шееле (1742-1786 гг.). Из-за большого разнообразия органических соединений каждое новое вещество представляло иной элементный состав, который соответствовал обобщенному наблюдению из «минеральной» химии. Количество изолированных органических соединений увеличилось вначале 1800-х годов, с помощью идентификации различных веществ.
В своей книге по истории химии Томас Томсон в 1830 году писал, что:
Берцелиус применил теорию атома также к растительному царству, проанализировав несколько растительных кислот, и показывая свою атомную конституцию, но здесь возникает трудность, которую в нынешнем состоянии наших знаний, мы не можем преодолеть. Есть две кислоты, которые состоят из точно таких же атомов. Теперь, как мы должны учитывать эту поразительную разницу в свойствах? Несомненно, различными способами, в которых атомы расположенных в каждом из них.
Затем Томсон использовал различные схемы атомных символов, используемых в то время, чтобы объяснить, почему две кислоты с одним и тем же элементарным составом, относящихся к геометрическим изомерам имеют разные физические и химические свойства.
До начала XIX века считалось, что эти химические вещества, обнаруженные в живых организмах, обладают особой жизненной силой, связанной с живыми существами, и что они нужны в живых системах для воспроизводства. В 1828 году Велер синтезировал образец мочевины, (NH2) 2CO (также CH4N2O), которая была неотличимой от мочевины, выделенной из биологической мочи.
Он подготовил это «животное» вещество из явно неорганического (минералогического) исходного вещества цианата аммония, (NH4)NCO (также CH4N2O), что является результатом объединения хлорида аммония и цианата серебра. Таким образом барьер между «живой» и «неживой» изомерией рухнул.
В цис-изомере две подобные группы остаются на одной стороне двойной связи, а в транс-изомере они остаются в противоположной стороне. Например, 2-бутен имеет два изомера цис и транс.
В цис-изомере две метильные группы и две водородные группы остаются в одной и той же стороне двойной связи, тогда как в транс-изомере они остаются в противоположной стороне.
Когда одна, или больше групп, связанных с двойной связью, не являются одинаковыми, изомеры называются E или Z. Для уведомления об этом типе пользователю потребуется указать формулы углеводородов, имеющих геометрические изомеры, и определяют атом с наивысшим приоритетом (самый высокий атомный номер), прикрепленный к каждой двойной связи C. Если два атома с наивысшим приоритетом остаются на той же стороне изомера, который обозначен как Z, и, если они находятся в противоположной стороне, обозначаются как E.

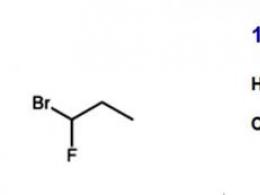
Например, 1 - бром - 1 - фторпропан имеет два изомера. В Z-1 - бром - 1 - фторпропане видно, что бром имеет более высокий приоритет или более высокий атомный номер (35), чем фтор (9), которые присоединены к С-1. Углерод имеет более высокое атомное число (6), чем водород (1), который присоединен к С-2 этого соединения. Поскольку атомы углерода с наивысшим приоритетом (из группы -CH3) и брома, присоединенные к этим двум атомам углерода, находятся на одной стороне, это соединение определяется как Z. С другой стороны, в E-1 - бром - 1 - фторпропан атомы с наивысшим приоритетом C и брома находятся в противоположной стороне, поэтому он называется E-изомером.
Углерод-углеродная двойная связь
Изомеры представляют собой две молекулы, которые имеют один и тот же атомный состав, но не идентичны. Атомы в двух изомерах могут быть связаны в другом порядке (структурная изомерия), или могут быть связаны таким же образом, но имеют другую ориентацию - пространственную стереоизомерию.
Структурный и геометрический изомер в особых случаях - стереоизомер, должен соответствовать двум требованиям:
- Существует ограниченное вращение в молекуле.
- Оба атома, участвующие в ограничительной связи, имеют к ним две различные функциональные группы.
Общим примером ограниченного вращения является углерод-углеродная двойная связь. Эти связи включают связь pi, в большинстве условий их разрывать не выгодно.

Геометрические изомеры имеют структуру, которая влияет на физические свойства соединения.
Система Cis/Trans
Именование Cis/Trans является самой простой системой соединений. Сначала идентифицируется самая длинная углеродная цепь в молекуле, а затем идентифицируются функциональные группы, представляющие интерес. В цис- изомере две рассматриваемые группы находятся на одной стороне двойной связи (cis означает "на той же стороне" на латыни). В транс- изомере две рассматриваемые группы находятся на противоположных сторонах двойной связи (транс означает поперек латинского языка). Например, два разных геометрических изомера бутена-2.

Оба атома с двойной связью имеют те же две группы, что и эти две группы, но они на одном из двойных углеродов отличаются друг от друга. Задача усложняется по мере того, как боковые цепи и функциональные группы становятся более сложными.
В официальной системе именования IUPAC используется обозначение E/Z. Специфической связи между цис/транс и E/Z нет, и эти две системы не являются взаимозаменяемыми. Обозначение E/Z использует правила приоритета Cahn-Ingold-Prelog, и считаются более надежными. Название IUPAC для фумаровой кислоты представляет собой транс-изомер с формулой HO2CCH=CHCO2H, а малеиновая кислота представляет собой цис-бутендиовую кислоту.

IUPAC - это Международный союз чистой и прикладной химии, который устанавливает международные правила и стандарты для обозначения химических веществ на всех языках.
В циклическом соединении вращение между углеродной одинарной связью ограничено. Таким образом, для этого типа соединений также возможна изомерия, если к каждому углероду присоединяются две разные группы. Существует два изомера 1,2-диметилциклопропана.

Один из них представляет собой цис-изомер, где две метильные группы находятся на одной стороне, а другая представляет собой транс-изомер, где две метильные группы находятся на другой стороне.
Геометрические изомеры различаются по своим физическим свойствам. Это связано с формой изомеров и общим дипольным моментом. Например, они отличаются точкой кипения. Точка кипения цис- и транс-изомеров 1,2-дихлорэтилена составляет 60,3 °C и 47,5 °C, соответственно.
В цис-изомере присутствие двух дипольных связей (C-Cl) дает общий молекулярный диполь. Это приводит к межмолекулярным диполь-дипольным силам. Для этой силы цис-изомер имеет большую температуру кипения, чем транс-изомер, где две дипольные связи (C-Cl) отменены из-за их положения в противоположном направлении.
Причина, по которой невозможно вращать углерод-углеродную двойную связь, состоит в том, что есть две связи, соединяющие атомы углерода вместе и придется разорвать связь pi. Связи pi образуются при боковом перекрытии между p-орбиталями. Если попытается повернуть углерод-углеродную двойную связь, p-орбитали больше не будут выстраиваться в линию, и поэтому связь pi будет нарушена. На это затрачивается энергии, и это происходит только в том случае, если соединение сильно нагревается.
Очень легко пропустить важные элементы геометрических изомеров во время построения структурных формул при сокращении. Например, очень заманчиво рисовать but-2-ene.Если пользователь напишет это неправильно, то соединение уже не будет изомером. Если есть хоть малейший намек на то, что может быть использован изомер, всегда необходимо использовать соединения, содержащие углерод-углеродные двойные связи, показывающие правильные углы (120°) вокруг атомов углерода на концах связи. Другими словами, необходимо использовать формат, показанный на рисунке.

Соединения, содержащие углерод-углеродную двойную связь, имеют ограниченное вращение. Чтобы получить изомеры, должны быть выполнены обязательные условия:
- ограниченное вращение, обычно, включающее углерод-углеродную двойную связь;
- две разные группы на левом конце связи и две разные группы на правом конце.
Не имеет значения, совпадают ли левые группы с правыми или нет.
Геометрические изомеры алкенов включают ряд соединений, которые состоят из атомов С и Н в цепи углерода. Эта группа включает гомологичную серию с формулой CnH2n. Простейший алкен - этен, имеет два атома С и формулу C2H4.

Структурная формула для этена представлена на рисунке выше. В более длинных алкеновых цепях дополнительные атомы углерода присоединены друг к другу с помощью одних ковалентных связей. Каждый атом углерода также присоединен к достаточным атомам водорода для получения в общей сложности четырех одиночных ковалентных связей.
В цепях с четырьмя и более атомами С, двойная связь может быть расположена в разных положениях, что приводит к образованию структурных изомеров. В дополнение к структурным изомерам алкены также образуют стереоизомеры. Поскольку вращение вокруг множественной связи ограничено, группы, присоединенные к атомам с двойной связью, всегда остаются в одинаковых относительных положениях.
Эти «заблокированные» позиции позволяют химикам идентифицировать различные изомеры из заместителей для того, чтобы определить, какое вещество имеет геометрические изомеры. Например, один структурный изомер C5H10 имеет следующие стереоизомеры.

Изомер слева, в котором два заместителя (метильная и этильная группы) находятся на одной стороне двойной связи, называют цис-изомер, тогда как изомер справа с двумя неводородными заместителями на противоположных сторонах является транс-изомером.
Например, хлор имеет приоритет, потому что он тяжелее. С правой стороны бром превосходит углерод. В-третьих, определяются положения двух атомов более высокого ранга. Если два атома находятся в цис-положении, расположение Z (с немецкого zusammen, что означает «вместе»). Если атомы, или группы, находятся в транс-положении, расположение E (от немецкого entgegen, что означает «противоположность»).
Геометрические изомеры бутен представляет собой алкен с жесткой двойной связью. Это означает, что на самом деле существует четыре изомера, а не три, в позиции двойной связи. Существует пятый и шестой углеводород того же состава, но они не являются алкенами, несмотря на ту же формулу.

Кольцевое образование циклобутана или метилциклопропана занимает пространство двух атомов водорода, как двойная связь, что приводит к тому, что они имеют формулы, идентичные различным бутенам.
Геометрические изомеры примеры:
- 1-butylene (1-butene);
- iso-butylene (2-methyl-propene);
- cis-2-butylene (cis-2-butene);
- trans-2-butylene (trans-2-butene).
И бонусы: циклобутан и метилциклопропан, - оба из которых имеют ту же эмпирическую формулу, что и изомеры бутена, но не являются алкенами. Первое имя - это «общее» или «тривиальное» имя, а имя в круглых скобках - это имя IUPAC.
Бутен имеет множество применений, от топлива в автомобиле до продуктовых сумок, которые носят ежедневно сотни миллионов жителей планеты. Химическая формула для бутена: C4H8, что означает, что она состоит из четырех атомов С и восьми атомов Н, соединение относится к алкену.
Существует несколько различных изомеров или молекулярных структур, которые могут образовывать это соединение (в скобках указаны названия IUPAC):
- alpha-butylene (but-1-ene);
- cis-beta-butylene - ((2Z)-but-2-ene);
- trans-beta-butylene - ((2E)-but-2-ene);
- isobutylene (2-methylprop-1-ene).

Хотя все они имеют одну и ту же формулу, их структуры различаются. Соотношения между каждым из этих геометрических изомеров в основном конституциональны, что означает, что они имеют одну и ту же молекулярную формулу, но разные связи. Исключением является цис-бета-бутилен и транс-бета-бутилен.
Многие знают, что транс-жиры вредны для человека, а ненасыщенные жиры полезные для него. Единственная разница между этими двумя жирами заключается в том, что у одного есть транс-связь, а у другого есть цис-связь, тем не менее эта небольшая дифференциация может существенно повлиять на функцию молекулы.
С цис-бета-бутиленом и транс-бета-бутиленом атомы находятся в одном порядке, но полярности различны. Цис-изомер является полярным, причем обе группы СН3 находятся на одной стороне. Это делает его действительно громоздким и сложным.Транс-изомер является неполярным, объемные группы CH3 чередуются, что дает больше места в молекуле. Это соотношение называется цис-транс-изомерией. Цис-изомеры являются полярными, тогда как транс-изомеры такими не являются.
Несмотря на то что каждый из этих изомеров бутена состоит из одних и тех же материалов, каждый из них имеет разные физические свойства. Например, точка кипения:
- Цис-бета-бутилен: 3,7 °C.
- Транс-бета-бутилен: 0,8 °C.
- Изобутилен: -6,9 °C.
- Альфа-бутилен: -6,3 °C.
Материал для производства пластмасс
Бутены представляют собой алкены с четырьмя атомами углерода, C4H8. Существует несколько различных структурных или конфигурационных изомеров бутена, в том числе геометрические и оптические изомеры. Все четыре бутена имеют схожие физические свойства, будучи бесцветными газами, тяжелыми в воде, хорошо растворимы в эфире и алканах. Различия в физических свойствах объясняются структурой молекул. Например, cis-But-2-en имеет более высокую температуру кипения, чем trans-But-2-en, потому что он является более сильным диполем.

Две алкильные группы цис-изомера работают со своим + I эффектом в одном направлении и тем самым усиливают, в то время как две алкильные группы транс-изомеров действуют в противоположных направлениях и, таким образом, ослабляют друг друга. Формулы углеводородов имеющих геометрические изомеры, указывают по стандартам IUPAC. But-1-en имеет такую низкую точку плавления, так как CC одинарная связь между вторым и третьим атомом углерода свободное вращения и этильная группа может, вращаться вокруг оси поворота во всех направлениях.
Это затрудняет классификацию молекулы в твердую кристаллическую структуру. Остальные три бутена с двойной связью между 2-м и 3-м атомом C, очень жесткие и могут быть легко классифицированы в кристаллической структуре. Поэтому они имеют относительно высокие температуры плавления. Эти аргументы не всегда действительны, так как на примере показан 2-Methyl-but-2-en (или изобутен). Две метильные группы с их + I-эффектами действуют в том же направлении, что и cis-But-2-en, и на самом деле должны быть улучшены. Тем не менее изобутен имеет очень низкую температуру кипения только -7 °C.
But-1-en и But-2-ene, используются для получения бутадиена и бутан- 2-ol. Кроме того, алкены используются в качестве алкилирующих агентов. Таким образом, из изобутена и изобутана получают важный топливный 2,2,4-Trimethyl-pentan, более известный как изооктан. Наконец, бутены являются исходными материалами для производства некоторых пластмасс, поскольку их легко полимеризовать. Известный пластик на But-1-en основе, является полибутеном-1, из которого производятся трубы.
Пентан, n-пентан, изопентан
Пентан, или n-пентан, является одним из насыщенных углеводородов алканов. Почти без запаха n-пентан является жидким в условиях окружающей среды и представляет собой изомер геракетхита из 3-х изомеров. Разветвленные жидкие изоалканы C5 - C16 все чаще используются в качестве топлива (Otto, Diesel). Кроме того, эти алканы присутствуют в отопительных маслах и смазочных маслах. Они обеспечивают полное горение. Прежде чем знать характеристику таких соединений нужно указать формулы углеводородов имеющих геометрические изомеры:
- Физическое состояние - жидкость.
- Цвет - бесцветный.
- Запах - почти нет.
- Легко воспламеним.
- Пары могут образовывать взрывоопасные смеси под воздействием воздуха.
- Водорастворимость очень низкая (практически нерастворимая).
- Очень неустойчивое соединение.
Наиболее важными источниками пентана являются нефтяные масла, которые значительно отличаются по своему составу в зависимости от их происхождения. Разделение происходит посредством фракционной перегонки. Здесь получают следующие фракции:
- Парафиновое масло (точка кипения> 320 °C).
- Нефть (точка кипения от 180 до 250 °C).
- Отопление / дизельное топливо (точка кипения от 250 до 320 °C).
- Сырой бензин (температура кипения до примерно 180 °C).
- В лигроине присутствуют разветвленные углеводороды (алканы) от C5 до C10.
- Сгорание пентана с кислородом (стехиометрическое).
- Конечными продуктами являются углекислый газ и вода. Формулы геометрических изомеров: C5H12 + 8O2 ⟹ 5CO2 + 6H2O.
| Теплотворная способность HU | Теплотворная способность HU [кВтч / кг] |
||
Геометрический изомер пентен-2 является универсальным растворителем. Он используется для вспенивания фенольной смолы и полистирола. Он также необходим в качестве эталонного вещества в газовой хроматографии, и в качестве пропеллента в баллонах для распыления.
Геометрические изомеры возникают, если свободное вращение атомов в молекуле ограничено вследствие наличия двойной связи. Примером такой пары изомеров могут служить малеиновая (12.23) и фумаровая (12.24) кислоты (цис- и транс- соответственно).
По химическому строению геометрические изомеры очень похожи, но они не являются зеркальными отображениями друг друга и не вращают плоскость поляризации света. Как правило, цис- и транс-изомеры значительно отличаются по физическим свойствам. Например, малеиновая кислота (12.23) плавится при 130 °С, величина ее рКа 1,9, она очень хорошо растворима в холодной воде (79 г на 100 мл); константы ее геометрического изомера - фумаровой кислоты (12.24) соответственно 287 °С, 3,0 и 0,7 г на 100 мл. Неудивительно, что геометрические изомеры обладают разными биологическими свойствами и поэтому очень важно при изучении химической формулы нового соединения учитывать все возможности существования изомерии такого типа.
Цис- и транс-изомеры можно легко разделить кристаллизацией или хроматографически. Общего метода для превращения одного изомера в другой не существует, однако при нагревании, как правило, образуется наиболее стабильный изомер, а под действием света - менее стабильный. Зрение человека зависит от превращения 11-цис-изомера ретиналя в 11-транс-форму под действием света. Как только возбуждающий луч света исчезает,
этот каротиноидный пигмент снова переходит в цис-форму, прерывая тем сй^ым идущий к мозгу импульс .
Цис- и транс-изомеры существуют и у плоского циклопентанового кольца, представляющего собой как бы большую двойную связь. Хотя циклогексановое кольцо вообще не плоское, оно тем не менее достаточно плоское для образования цис- и трансизомеров. Так, существуют и доступны как цис- (12.25), так и транс- (12.26) формы диаминоциклогексана. Одна и та же молекула может образовывать и геометрические, и оптические изомеры. Например, транс-изомер (12.26) может быть разделен на (S,S) (12.27) и (R,R) (12.28) хиральные изомеры. Однако цис-изомер на хиральные формы разделен быть не может, так как в нем существует плоскость симметрии. У бензольного кольца нет геометрических изомеров, так как у каждого атома углерода кольца только один заместитель.
Стереоизомеры 1,2-диаминоцинлогенсана
Иногда бывает трудно выбрать два из четырех заместителей при двойной связи для определения цис- или транс-конфигурации. Правило последовательности предписывает выбирать заместителей с наиболее тяжелыми атомами, при этом цис-форма обозначается буквой Z (от немецкого слова zusammen), а трансформа- буквой Е (entgegen). Иногда в названиях соединений, в которых геометрическая изомерия может проявиться многократно, заместитель, имеющий самый маленький номер (по правилу нумерации), обозначают буквой г, а обозначения с-(цис) и t-(транс) перед другими заместителями показывают их положение по отношению к г-заместителю.
Аналогично индол-3-илуксусной кислоте (4.82), стимулирующей рост растительных клеток, могут действовать и другие карбоновые кислоты, карбоксильная группа которых находится под углом к плоскости ароматического кольца. Геометрическая изомерия ограничивает возможность такого расположения двух заместителей, поэтому из коричных кислот активен только цисизомер . У 2-фенилциклопропан-1- карбоновой и 1,2,3,4-тетрагидронафталиден-1-уксусной кислот также активны только цис-изомеры . На молекулярных моделях видно, что кольцо и карбоксильная группа в транс-изомере (неактивном) этих веществ лежат в одной плоскости, в то время как в цис-форме (активной) они некопланарны. Впервые указал на эту связь между
некопланарностью и стимулирующей рост активностью Veidstra. Некопланарность может возникнуть и вследствие стерических препятствий. Так, бензойная кислота имеет плоскую форму и не активна, а 2,6-дихлорбензойная и 8-метил-1-нафтойная кислоты непланарны и биологически активны .
В аналогах ауксинов карбоксильная группа может быть заменена и на другие электроноакцепторные группы (-CN, -NO 2 , -SO3H), при этом биологическая активность лишь незначительно уменьшается. О связи между структурой и действием в этой серии см. Koepfli, Thimann, Went (1938) и Veidstra (1963).
Геометрическая изомерия стероидов заслуживает специального рассмотрения. На формуле (12.29) приведена общая структура этой группы природных насыщенных соединений (показана нумерация атомов углерода и буквенные обозначения четырех циклов). В природных стероидах кольца В и С находятся в транс-сочленении, причем оба они закреплены в конформации кресла. В сердечных гликозидах сочленение циклов С и D имеет цис-конфигурацию, но в гормонах животных, стеринах и желчных кислотах - транс-сочленение. У большинства биологически активных стероидов кольца А и В находятся в транс-сочленении («5а»-ряд, называвшийся ранее «алло»). Каждое из колец в молекуле стероидов образует складки, что хорошо видно на боковой проекции формулы (12.30).

Обозначение «5а» говорит о том, что атом водорода в положении 5 находится ниже общей плоскости колец. Все заместители, расположенные ниже этой плоскости, обозначаются символом «а», а выше - символом «р». а-Заместители обозначают пунктирными линиями, а ^-заместители - сплошными. Символы а- и ^-используют и для других полициклических соединений, например, тритерпенов и алкалоидов. Сложность строения этих соединений затрудняет использование R- и S-номенклатуры.
Как правило, у млекопитающих высокая биологическая активность стероидных соединений связана с отсутствием а-заме- стителей в положениях 1, 9, 11-13, 17 и отсутствием р-замести- телей в положениях 4-8, 14, 15. Боковая проекция молекулы гидрокортизона иллюстрирует это правило . Первой стадией в биологическом действии стероидных гормонов является их влияние на специфический транспорт белков (разд. 2.4). Предполагают, что с белками стероиды взаимодействуют плоской нижней стороной (a-поверхность) молекулы.
Различные стероиды отличаются друг от друга в основном заместителями R 1 , R 2 и R 3 (12.29), но иногда и степенью нена- сыщенности или наличием других заместителей вне колец. Для того чтобы стероид обладал прогестиновой, андрогенной и кор- тикоидной активностью, как правило, необходимо наличие циклогексеноновой структуры кольца А. Для проявления активности кортизонового типа необходимы атомы кислорода в положениях 3, 11 и 17 и характеристичная группа -СО-СН 2 ОН в положении 17. Андрогенная и кортикоидная активность в большей степени зависит от этих деталей строения молекулы, однако прогестиновая активность сохраняется, если ацетильная группа в положении 17 находится в a-конфигурации, не встречающейся в природных соединениях, а замена метильной группы в положении 18 на этильную приводит даже к усилению этой активности (пероральный контрацептив норгестрел).
Из всех стероидных гормонов наименее жесткие требования к структуре предъявляют соединения, обладающие эстрогенной активностью. При условии ароматизации кольца А и наличии кислой гидроксильной группы в положении 3 строение остальной части молекулы имеет второстепенное значение. В 1938 г. появились простые высокоэффективные бензольные аналоги стероидных эстрогенов. Хотя считалось, что их молекулы по форме похожи на молекулы стероидов, в действительности между ними не так уж много общего. По данным рентгеноструктурного анализа молекула диэтилстильбэстрола (12.31) имеет транс-конфигурацию, искаженную из-за стерических затруднений, создаваемых метиленовыми фрагментами двух этильных групп. Поэтому два бензольных кольца образуют с этиленовым фрагментом двугранный угол 63°, что делает форму молекулы совершенно не похожей на стероидную. Однако в этих молекулах примерно одинаково расстояние между атомами кислорода: 1,21 нм в диэтилстильбэстроле и от 1,07 до 1,11 нм в стероидных эстрогенах, но все эти молекулы слишком жесткие и поэтому не способны взаимодействовать с одним и тем же рецептором, в котором фиксировано расстояние между точками связывания. Известно, что для проявления эстрогенной активности необходимо образование двух водородных связей рецептора с атомами кислорода лиганда, следовательно, рецептор должен обладать определенной гибкостью . Oki, Urushibara (1952) впервые отметили, что действие диэтилстильбэстрола связано и с толщиной его молекулы, которая составляет 0,45 нм и равна толщине молекул стероидных эстрогенов .

Диэтилстильбэстрол 3,4-ди (4-гидроксифенил) гекс-3-ен
(12.31), эффективный и недорогой заменитель основного женского гормона эстрадиола (12.32), появился в 1938 г. . Этот синтетический лекарственный препарат, отличающийся от природного гормона высокой эффективностью при пероральном применении и большей длительностью действия, стал основным препаратом в эндокринной терапии. Некоторое недоверие к этому препарату возникло на основании двух факторов: во-первых, его неограниченно применяли для увеличения веса сельскохозяйственных животных, а во-вторых, были отмечены случаи заболевания раком у женщин, матери которых принимали его во время беременности. Несмотря на это, диэтилстильбэстрол продолжают широко применять и считают безопасным средством; его не назначают только в первые три месяца беременности (что, кстати, в равной степени относится и к природному гормону). О применении его фосфата для лечения рака предстательной железы см. разд. 4.2. Сходными эстрогенными свойствами обладает и дигидропроизводное диэтил- стильбэстрола-синэстрол (12.33, а) (конфигурация 3R, 4S). С эстрогенсвязывающим белком (разд. 2.4) он соединяется сильнее, чем сам диэтилстильбэстрол, а еще сильнее взаимодействует с этим белком его низший гомолог-норгексэстрол (12.33, б) .
Сердечные гликозиды рассматриваются в разд. 14.1. Подробное изложение химии и стереохимии стероидов см. Shoppee (1964), биохимии и фармокологии - Briggs, Christie (1977).
Геометрическая изомерия 4-аминокротоновой кислоты, которая помогла определить активную конформацию нейромедиатора гамма-аминомасляной кислоты, рассматривается в разд. 12.7.
Причиной возникновения геометрической изомерии является отсутствие свободного вращения вокруг ст-связи. Этот вид изомерии характерен для соединений, содержащих двойную связь, и для соединений алициклического ряда.
Геометрические изомеры - это вещества, имеющие одинаковую молекулярную формулу, одинаковую последовательность связывания атомов в молекулах, но отличающиеся друг от друга различным расположением атомов или атомных групп в пространстве относительно плоскости двойной связи или плоскости цикла.
Причиной возникновения данного вида изомерии является невозможность свободного вращения вокруг двойной связи или ст-связей, образующих цикл.
Например, бутен-2 СН3-СН=СН-СН3 может существовать в виде двух изомеров, которые различаются расположением ме-тильных групп в пространстве относительно плоскости двойной связи:
или т,2-димтетилцитктопропан существует в виде двух изомеров,
которые различаются расположением метильных групп в пространстве относительно плоскости цикла:

/для обозначения конфигурации геометрических изомеров используют цис-, транс-систему. Если одинаковые заместители
3. Изомерия органических соединений. Пространственное строение молекул
ра^п^лиж^пш по одпу сторопу от ттлоскости двойпой ^dajw или
цикла, копфигурацию обозпачают цис-, если по разпые сторо-пы, - транс-.
Для соедипепий, у которых при атомах углерода с двойпой связью паходятся различпые заместители, примепяют Е^-систе-му обозпачепий.
EZ-Система является более общей. Опа примепима к геометрическим изомерам с любым пабором заместителей. В оспове этой системы лежит старшипство заместителей, которое определяют у каждого атома углерода отдельпо. Если старшие заместители из каждой пары расположепы по одпу сторопу от двойпой связи, коп-фигурация обозпачается буквой Z (от пем. zusammen - вместе), если по разпые сторопы,- буквой Е(от пем. entgegen - папротив).
Так, для 1-бром-1-хлорпропепа возможпо два изомера:

старшим! заместителем у одного атома углерода является ме-
тильная группа (заместители 1Н и 6СН3), а у другого - атом брома (заместители 17С1 и 35Вг). В изомере I старшие заместители расположены по одну сторону от плоскости двойной связи, ему приписывают Z-конфигурацию, а изомеру II - Е-конфигурацию (старшие заместители расположены по разные стороны плоскости двойной связи).
Геометрические изомеры имеют разные физические свойства (температуру плавления и кипения, растворимость и так далее), спектральные характеристики и химические свойства. Такое различие в свойствах позволяет довольно легко установить их конфигурацию с помощью физических и химических методов.
Изомерия лигандов
Изомерия лигандов подразделяется на связевую (которая определяется разным типом координации одного и того же лиганда), и собственно изомерию лиганда.
Примерами связевой изомерии может служить существование нитро- и нитрито-комплексов кобальта(III) состава K 3 и K 3 , в которых координация лиганда NO 2 - осуществляется, соответственно, через атом азота или атом кислорода. Другой пример – координация тиоцианат-иона NCS - через атом азота или через атом серы, с образованием тиоцианато-N- или тиоцианато-S-комплексов.
Кроме того, лиганды сложного строения (например, аминокислоты) могут сами по себе образовывать изомеры, координация которых ведет к образованию комплексов одинакового состава с разными свойствами.
Геометрическая изомерия вызвана неодинаковым размещением лигандов во внутренней сфере относительно друг друга. Необходимым условием геометрической изомерии является наличие во внутренней координационной сфере не менее двух различных лигандов. Геометрическая изомерия проявляется преимущественно у комплексных соединений, имеющих октаэдрическое строение, строение плоского квадрата или квадратной пирамиды.
Комплексные соединения с тетраэдрическим, треугольным и линейным строением геометрических изомеров не имеют, поскольку места расположения лигандов двух разных видов вокруг центрального атома равноценны.
Комплексы, имеющие строение плоского квадрата, при наличии двух разных лигандов L ′ и L ′′ уже могут иметь два изомера (цис- и транс-):
Примером комплексного соединения, имеющего цис- и транс-изомеры, может служить дихлородиамминплатина(II):
Отметим, что комплексное соединение состава со структурой плоского квадрата не может иметь изомеров: положение лиганда L ′′ равновероятно в любом углу квадрата. Когда же появляется два разных лиганда, то уже возможно существование двух изомеров (цис- и транс-), отличающихся по свойствам. Так, цис-дихлородиамминплатина (II) – оранжево-желтые кристаллы, хорошо растворимые в воде, а транс-дихлородиамминплатина(II) – кристаллы бледно-желтого цвета, растворимость которых в воде несколько ниже, чем у цис-изомера.
С увеличением числа различных лигандов во внутренней сфере растет число геометрических изомеров. Для хлорида нитро(гидроксиламин)аммин(пиридин)платины(II) Cl получены все три изомера:
Октаэдрические комплексы могут иметь множество изомеров. Если в комплексном соединении такого рода все шесть лигандов одинаковы () или отличается от всех остальных только один (), то возможность различного расположения лигандов по отношению друг к другу отсутствует. Например, у октаэдрических соединений любое положение лиганда L ′′ по отношению к остальным пяти лигандам L ′ будет равноценным и поэтому изомеров здесь не должно быть:
Появление двух лигандов L ′′ в октаэдрических комплексных соединениях приведет к возможности существования двух геометрических изомеров . В этом случае появляются два различных способа расположения лигандов L ′′ друг относительно друга. Например, катион дигидроксотетраамминкобальта(III) + имеет два изомера:
При попытке найти какое-нибудь еще взаимное расположение лигандов H 3 N и OH - , которое отличалось бы от указанных выше, мы всегда придем к строению одного из уже приведенных.
При увеличении в комплексе числа лигандов, имеющих разный химический состав, число геометрических изомеров быстро растет. У соединений типа будет четыре изомера, а у соединений типа , содержащих шесть разных лигандов, число геометрических изомеров достигает 15. Подобные комплексные соединения пока еще мало изучены.
Геометрические изомеры существенно отличаются по физико-химическим свойствам, таким как цвет, растворимость, плотность, кристаллическая структура и т.д.
Изомеры - вещества с одинаковым строением молекулы, но разными химическим строением и свойствами.
Виды изомерии
I . Структурная - заключается в различной последовательности соединения атомов в цепи молекулы:
1) Изомерия цепи
Следует отметить, что атомы углерода в разветвленной цепи различаются типом соединения с другими углеродными атомами. Так, атом углерода, связанный только с одном другим углеродным атомом, называется первичным , с двумя другими атомами углерода - вторичным , с тремя - третичным , с четырьмя - четвертичным .
2) Изомерия положения

3) Изомерия межклассовая
4) Таутомерия
Таутомери́я (от греч. ταύτίς — тот же самый и μέρος — мера) — явление обратимой изомерии, при которой два или более изомера легко переходят друг в друга. При этом устанавливается таутомерное равновесие, и вещество одновременно содержит молекулы всех изомеров в определённом соотношении. Чаще всего при таутомеризации происходит перемещение атомов водорода от одного атома в молекуле к другому и обратно в одном и том же соединении.
II. Пространственная (стерео) - обусловлена различным положением атомов или групп относительно двойной связи или цикла, исключающих свободное вращение соединённых атомов углерода
1. Геометрическая (цис -, транс - изомерия)

Если атом углерода в молекуле связан с четырьмя различными атомами или атомными группами, например:
то возможно существование двух соединений с одинаковой структурной формулой, но отличающихся пространственным строением. Молекулы таких соединений относятся друг к другу как предмет и его зеркальное изображение и являются пространственными изомерами.
Изомерия этого вида называется оптической, изомеры - оптическими изомерами или оптическими антиподами:
Молекулы оптических изомеров несовместимы в пространстве (как левая и правая руки), в них отсутствует плоскость симметрии.
Таким образом,
- оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение.

Оптические изомеры аминокислоты
3. Конформационная изомерия
Следует отметить, что атомы и группы атомов, связанные друг с другом σ -связью, постоянно вращаются относительно оси связи, занимая различное положение в пространстве друг относительно друга.
Молекулы, имеющие одинаковое строение и различающиеся пространственным расположением атомов в результате вращения вокруг С-С связей, называются конформерами.
Для изображения конформационных изомеров удобно пользоваться формулами - проекциями Ньюмена:
Явление конформационной изомерии можно рассмотреть и на примере циклоалканов. Так, для циклогексана характерны конформеры:
Рассмотренные нами ранее виды формул, описывающих органические вещества, показывают, что одной молекулярной может соответствовать несколько разных структурных формул.
Например, молекулярной формуле C2 H6 O соответствуют два вещества с разными структурными формулами - этиловый спирт и диметиловый эфир. Рис. 1.
Этиловый спирт - жидкость, которая реагирует с металлическим натрием с выделением водорода, кипит при +78,50С. При тех же условиях диметиловый эфир - газ, не реагирующий с натрием, кипит при -230С.
Эти вещества отличаются своим строением - разным веществам соответствует одинаковая молекулярная формула.

Рис. 1. Межклассовая изомерия
Явление существования веществ, имеющих одинаковый состав, но разное строение и поэтому разные свойства называют изомерией (от греческих слов «изос» - «равный» и «мерос» - «часть», «доля»).
Типы изомерии
Существуют разные типы изомерии.
Структурная изомерия связана с разным порядком соединения атомов в молекуле.
Этанол и диметиловый эфир - структурные изомеры. Поскольку они относятся к разным классам органических соединений, такой вид структурной изомерии называется еще и межклассовой . Рис. 1.
Структурные изомеры могут быть и внутри одного класса соединений, например формуле C5H12 соответствуют три разных углеводорода. Это изомерия углеродного скелета . Рис. 2.

Рис. 2 Примеры веществ - структурных изомеров
Существуют структурные изомеры с одинаковым углеродным скелетом, которые отличаются положением кратных связей (двойных и тройных) или атомов, замещающих водород. Этот вид структурной изомерии называется изомерией положения .
Рис. 3. Структурная изомерия положения
В молекулах, содержащих только одинарные связи, при комнатной температуре возможно почти свободное вращение фрагментов молекулы вокруг связей, и, например, все изображения формул 1,2-дихлорэтана равноценны. Рис. 4

Рис. 4. Положение атомов хлора вокруг одинарной связи
Если же вращение затруднено, например, в циклической молекуле или при двойной связи, то возникает геометрическая или цис-транс изомерия. В цис-изомерах заместители находятся по одну сторону плоскости цикла или двойной связи, в транс-изомерах - по разные стороны.
Цис-транс изомеры существуют в том случае, когда с атомом углерода связаны два разных заместителя. Рис. 5.



Рис. 5. Цис- и транс- изомеры
Еще один тип изомерии возникает в связи с тем, что атом углерода с четырьмя одинарными связями образует со своими заместителями пространственную структуру - тетраэдр. Если в молекуле есть хотя бы один углеродный атом, связанный с четырьмя разными заместителями, возникает оптическая изомерия . Такие молекулы не совпадают со своим зеркальным изображением. Это свойство называется хиральностью - от греческого с hier - «рука». Рис. 6. Оптическая изомерия характерна для многих молекул, входящих в состав живых организмов.
|
|
|
Рис. 6. Примеры оптических изомеров
Оптическая изомерия называется также энантиомерией (от греческого enantios - «противоположный» и meros - «часть»), а оптические изомеры - энантиомерами . Энантиомеры оптически активны, они вращают плоскость поляризации света на один и тот же угол, но в противоположные стороны: d- , или (+)-изомер, - вправо, l- , или (-)-изомер, - влево. Смесь равных количеств энантиомеров, называемая рацематом , оптически недеятельна и обозначается символом d,l- или (±).
ИСТОЧНИКИ
источник видео - http://www.youtube.com/watch?v=mGS8BUEvkpY
http://www.youtube.com/watch?t=7&v=XIikCzDD1YE
http://interneturok.ru/ru/school/chemistry/10-klass - конспект
источник презентации - http://ppt4web.ru/khimija/tipy-izomerii.html
http://www.youtube.com/watch?t=2&v=ii30Pctj6Xs
http://www.youtube.com/watch?t=1&v=v1voBxeVmao
http://www.youtube.com/watch?t=2&v=a55MfdjCa5Q
http://www.youtube.com/watch?t=1&v=FtMA1IJtXCE
источник презентации - http://mirhimii.ru/10class/174-izomeriya.html